Mal de las Chagas
Por: Dr.
Seambelar
 Con
motivo del brote de le Enfermedad de Chagas ocurrida en Brasil,
haremos algunas consideraciones sobre la misma y adjuntamos datos
extraídos del diario "La Nación" y un meduloso
trabajo científico del Dr. Sergio Sosa Estani
Con
motivo del brote de le Enfermedad de Chagas ocurrida en Brasil,
haremos algunas consideraciones sobre la misma y adjuntamos datos
extraídos del diario "La Nación" y un meduloso
trabajo científico del Dr. Sergio Sosa Estani
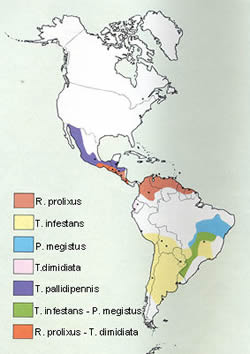
Comenzaremos con el mapa de distribución de los distintos
tipos de vectores que transmiten la enfermedad de Chagas en América.
Enfermedad de Chagas
Esta enfermedad es producida por el Tripanosoma Cruzi, este agente
causal de la enfermedad infecta diversas especies de insectos, llamados
vectores, que se nutren de sangre, ya sea de animales o seres humanos
infectados, que tengan parásitos circulantes en la sangre
llamados Tripomastigotos, estos parásitos ingeridos se transforman
en el intestino medio del insecto en Epimastigotos, que se multiplican
en el intestino medio del agente vector y en este se transforman
nuevamente en Tripomastigotos en la parte caudal del intestino,
cerrando de esta manera el ciclo evolutivo, cuando este agente infectado
chupa sangre para alimentarse, defeca depositando las heces sobre
la piel, o las conjuntivas del ojo, las formas metacíclicas
infecciosas, de esta manera llega el Trypanosoma Cruzi a un organismo
vertebrado, los parásitos pueden penetrar en diversos tipos
de células transformándose aquí en Amastigotas
Intracelulares, dentro de dichas células crecen, se reproducen
se alargan y se transforman en Tripomastigotos Móviles y
hacen estallar las células que lo contienen pasando a la
circulación sanguínea, o penetrando a nuevas células.
y así sucesivamente. El Trypanosoma Cruzi llega generalmente
de esta manera al organismo, pero puede también hacerlo,
cuando el huésped receptor ingiere comidas infectadas por
el Trypanosoma Cruzi, como ocurrió en el caso del brote en
Brasil, que llegó al organismo humano por ingesta de cañas
de azúcar contaminadas por heces infectadas con el Trypanosoma
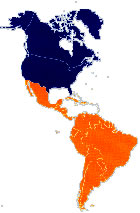
Cruzi. Esta enfermedad se extiende desde Norteamérica hasta
Chile y la Argentina, extendiéndose en este país hasta
la Pcia. de Neuquén en el Sur. Los síntomas de la
enfermedad, cuya incubación dura alrededor de 20 días,
son fiebre, decaimiento y dolor muscular
El Ministerio de Salud de la Nación confirmó ayer
que "hasta ahora, no hubo ningún caso argentino"
por el brote de la enfermedad del Mal de Chagas que desde la semana
última afecta al estado de Santa Catarina, ubicado al sur
de Brasil.
El rebrote de la enfermedad, que en América latina afecta
a 16 millones de personas, habría utilizado una vía
de contagio poco común: la digestiva. Una bebida hecha a
base de jugo de caña (garapa) habría estado infectada
con el parásito que causa el mal.
 Otras
formas de propagación de la enfermedad
Otras
formas de propagación de la enfermedad
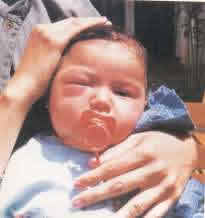
Por vía Transplacentaria: La infección prenatal por
pasaje transplacentario de tripanosomas desde la circulación
materna con infección aguda o crónica, es posible,
pero no obligada. Se ha verificado nacimiento de niños no
infectados, aun en presencia de placenta con elevado parasitismo.
Se ha comprobado igualmente la inversa: madre con bajísima
parasitemia, placenta sin parásitos y nonato con enfermedad
de Chagas franca (distrofia, edemas, fiebres y parasitemia elevada).
Muchas de las formas de enfermedad de Chagas en lactantes, sin
puerta de entrada y sin seguridad de exposición a vinchucas,
son de transmisión transplacentaria; hijos de madres que
apenas dan una reacción de desviación del complemento
positiva.
Por hemotransfusion: Otro considerable numero de infecciones se
produce mediante la transfusión de sangre proveniente de
dadores con infecciones ignoradas, generando cuadros clínicos
atípicos. Si bien se han registrado casos mortales fulminantes,
la mayoría mejoran espontáneamente, aun en presencia
de alta parasitemia inicial. La posibilidad de evolución
esta condicionada por la cepa infectante y la inmunidad del receptor.
Por leche maternal: La posibilidad de infección del hijo
por la leche de madre que padece la enfermedad de Chagas es posible;
ha sido verificada clínicamente y cuenta con ratificación
experimental. Sin embargo, su ocurrencia es excepcional y muchos
especializados consideran que es un riesgo remoto. No obstante,
es prudente que el hijo de una mujer que sufre enfermedad de Chagas
aguda, no sea amamantado por su madre.
Por contaminación accidental en el Laboratorio: Son múltiples
los casos conocidos de enfermedad de Chagas por infección
accidental en laboratorios médicos, por manipulación
de vinchucas y animales infectados, cultivos de T Cruzi o material
biológico proveniente de enfermos graves o de animales infectados.
De estas desgracias es conocida la infección fulminante que
costo la vida al argentino Mario Fatala Chaben.
Por manejo de animales contaminados: Se han relatado casos contraídos
al desollar animales silvestres o semidomesticos enfermos ( entre
ellos los cuyes, criados para alimentación familiar en ciertas
regiones de Perú y Bolivia). Se ha encontrado el Tripanosoma
en la saliva de perros infectados con alta parasitemia; el manejo
promiscuo de canes y gatos con infección natural acentuada
puede ser medio de contagio.
En Brasil ya se registraron seis víctimas mortales y se
detectaron 25 personas infectadas. Las autoridades sanitarias del
estado afectado estiman que unas 50.000 personas pudieron estar
expuestas al Trypanosoma Cruzi , el parásito responsable
de la enfermedad, que contamina a través de las heces de
la vinchuca.
Nosología General
La enfermedad de Chagas o tripanosomiasis Cruzi humana, es una parasitosis
producida por el protozoo flagelado Trypanosoma Cruzi, hematófilo
pero que se reproduce en los tejidos, por la división binaria,
múltiple y progresiva, pasando por una forma no flagelada:
amastigote.
Se transmite entre diversos hospedadores animales, mamíferos
silvestres y domésticos, a sus congéneres por insectos
hematófagos, conocidos en la Argentina y países vecinos
con el nombre vulgar de "vinchucas".
 Vinchuca
Vinchuca
Es el vector de la enfermedad. Como en todos los insectos, el cuerpo
de la vinchuca esta compuesto de tres regiones: cabeza, tórax
y abdomen. Exteriormente podemos observar que la cabeza posee los
órganos sensoriales, en el tórax están insertados
los órganos locomotores y en el abdomen, el aparato reproductor
y las aberturas respiratorias.
La cabeza es alargada, fusiforme en la mayoría de las especies.
Posee un par de ojos compuestos, que son globosos y salientes, un
par de ojos menores, los ocelos y un par de antenas, órganos
receptores de sensaciones que no han sido bien determinadas aun.
En la cara ventral del tórax se insertan las patas que
son delgadas y relativamente largas. Gran parte del dorso del abdomen
esta cubierto por alas. Queda descubierto el conexivo, que es el
reborde que rodea el abdomen y se destaca por mostrar manchas transversales
claras, característica muy importante para identificar a
las vinchucas.
La vinchuca Domiciliaria
Hay mas de un centenar de especies de vinchucas, 16 de ellas habitan
en nuestro país, pero no todas tienen importancia epidemiológico
en la transmisión del Trypanosoma Cruzi, que es un parásito
unicelular microscópico, agente casual de la Enfermedad de
Chagas.
Un grupo de especies tiene hábitos silvestres y es vector
del Trypanosoma entre los mamíferos salvajes. Otro grupo
suele invadir la zona peri-domiciliaria, estableciéndose
en gallineros, corrales, conejeras, etc; se alimenta sobre los animales
domésticos, participando en la transmisión del parásito
al perro, gato y otros mamíferos que se crían cerca
de las viviendas: estas especies de vinchucas están muy cerca
del hombre, pero no llegan a invadir las viviendas del hombre y
por lo tanto no se alimentan sobre el ni le transmiten la enfermedad.
En nuestro país hay una sola especie de vinchuca que convive
habitualmente con el hombre en el interior de las viviendas y se
alimenta con su sangre: es Triatoma infestans, llamada popularmente
chinche gaucha, vinchuca negra, o simplemente vinchuca. A esta especia
nos referimos.
El adulto mide entre 2 ½ y 3 cm de largo; el macho es algo
menor que la hembra. Una manera bastante segura de diferenciar la
vinchuca domiciliaria de otras especies, es observar las bases de
las patas, que presenta un color amarillo que se destaca del negro
de la coloración general del insecto..
 Desarrollo
de la vinchuca
Desarrollo
de la vinchuca
Se reproduce por huevo. La hembra pone hasta 200 de forma elíptica
y de color blanco cuando son recién puestos. Luego este color
va cambiando a rosado al adelantar el desarrollo del embrión,
cuya evolución se completa entre 20 y 50 días, según
sea la temperatura. Los huevos son depositados en la tierra, en
las grietas de las paredes y en otros lugares mas o menos ocultos.
Desde que sale el huevo hasta que alcanza el estado adulto, el
insecto experimenta una serie de transformaciones ( proceso de metamorfosis,
que tiene una duración variable en relación con la
temperatura, la humedad y la alimentación).
Al nacer; el insecto tiene unos tres milímetros de largo
y es parecido al adulto, pero carece de alas. En esta primera fase
del proceso de metamorfosis, recibe el nombre de chinche pila. Unas
semanas después, la ninfa muda de piel y aumenta de tamaño
pero sigue careciendo de alas. Estas mudas se repiten en numero
de cinco: cada una de ellas da origen a una ninfa cada vez mayor.
Con la ultima muda aparecen las alas y el insecto adquiere su aspecto
definitivo.Todo este proceso dura alrededor de 7 meses
Epidemia - Pandemia - Endemia
El termino epidemia proviene del griego epi:sobre y demos:pueblo,
y significa aparición súbita de una enfermedad, que
ataca un gran numero de individuos que habitan una región
determinada. Para que una enfermedad sea considerada epidemia, la
cantidad de afectados debe superar el numero habitual de casos esperados.
Como ejemplos de epidemias en nuestro país, se pueden mencionar
la de la poliomielitis, ocurrida en el año 1956, y la de
la gripe, en el año 1968.
Si una enfermedad persiste durante años en un lugar determinado,
ya no se habla de epidemia, sino de endemia ( del griego en:en y
demos:pueblo). El numero de afectados puede, o no, ser elevado.
Una endemia es, por lo tanto, una enfermedad "crónica"
en una zona determinada. En nuestro país, el Mal de Chagas
( del cual luego explicaremos) y la hidatidosis, entre otras enfermedades,
son consideradas como endemias.
Por ultimo, cuando una enfermedad se extiende a través
de varios países y continentes, traspasa todas las fronteras,
supera el numero de casos esperados y persiste en el tiempo, se
habla de pandemia ( del griego pan:todo, demos:pueblo). La peste
bubónica y la viruela son ejemplos históricos de pandemias.
La epidemiología estudia las formas en que las enfermedades
afectan a un grupo de personas, en un lugar y un tiempo determinado.
Mal de Chagas Historia
Por el numero de enfermos y la amplitud del área que abarca,
por la gravedad de las alteraciones cardiacas y de otros tipos que
ocaciona y por su carácter endémico, la enfermedad
de Chagas es uno de los principales problemas de la salud publica
en nuestro país.
El Dr. Carlos Chagas (1879-1934), celebre investigador brasileño;
realizo un descubrimiento que tiene un historial muy interesante,
pocas veces repetido: el parásito fue encontrado antes que
la enfermedad.
Cuando este investigador fue enviado a Lassance estado de Minas
Gerais, Brasil- para estudiar algunos problemas sanitarios encontró
que los "barbeiros", nombre popular de las vinchucas en
el Brasil, tenían en sus deyecciones unos protozoarios que
identifico como parásitos del genero Trypanosoma, de que
se conocían algunas especies en otras partes del mundo.
La nueva especie la denomino Trypanosoma Cruzi en homenaje a Osvaldo
Cruz, su maestro.
En la Argentina, la enfermedad de Chagas fue estudiada principalmente
por el Dr. Salvador Mazza, trabajador infatigable, quien mostró
su gran importancia sanitaria, describió formas clínicas
y difundió sus análisis a través de la Misión
de Estudios de Patología Regional Argentina, que fundara.
Para el estudio y control de esta enfermedad, la Secretaria de
Salud Publica de la Nación ha creado el Instituto Nacional
de Diagnostico e Investigación de la enfermedad de Chagas
"Dr. Mario Fatala Chaben" y un Servicio Nacional de Lucha
con programas en las provincias endémicas.
 Evolución
y Manifestación del Mal de Chagas
Evolución
y Manifestación del Mal de Chagas
Señalaremos en primer lugar su evolución en 3 periodos:
1) AGUDO o de comienzo que dura alrededor de 20 a 30 días;
2) INTERMEDIO o DE LATENCIA, cuya duración es variable y
puede alcanzar varios años;
3) CRONICO, con una duración que depende de la gravedad que
alcance el proceso.
Periodo Agudo: Signo de Romaña
La mayor parte de los afectados por la enfermedad son niños,
no porque estos sean mas susceptibles que los adultos, sino simplemente
por tener antes en la vida la posibilidad de ser infectados por
la vinchuca.
El periodo de incubación ( que es el lapso que media entre
la introducción del Trypanosoma en el organismo y la aparición
de los primeros síntomas) es de duración variable,
con un termino medio de una semana. El inicio de las molestias es
súbito, presentando el enfermo fiebre, escalofríos,
dolor de cabeza y de los músculos del cuerpo, malestar general
e inapetencia. Algunas veces hay signos en el organismo que delatan
la puerta de entrada de la infección: son el complejo oftalmoganglionar
y los habones de inoculación.
El complejo oftalmoganglionar o signo de eje, representa una manifestación
de valor diagnostico. Lamentablemente se ve solo en no mas del 4%
del total de formas agudas. Se caracteriza por: comienzo habitualmente
súbito, hinchazón elástica e indolora de los
párpados superior e inferior de un solo ojo, que toman color
morado ( como si fuera un "ojo en compota"); conjuntivas
rojas; hinchazón moderada del lado facial correspondiente
al ojo afectado. Esta inflamación ocular desaparece lentamente
en el curso de la fase aguda de la afección.
Los "habones de inoculación", otro signo de puerta
de entrada de la infección, consisten en zonas de endurecimiento
cutáneo que pueden aparecer en cualquier lugar del cuerpo,
especialmente en las partes descubiertas. Estas zonas generalmente
tienen un color rojo y alta temperatura local; surgen como si brotara
del interior de la piel. Son poco dolorosos. El habón de
inoculación tiende a desaparecer espontáneamente al
cabo de 2 o 3 meses; queda en ese sitio una pigmentación
característica.
Periodo de Latencia
Pasado el primer mes, el enfermo entra en un segundo periodo, o
de latencia; este periodo puede durar años y durante ese
tiempo no hay ningún síntoma; solamente se puede poner
en evidencia la enfermedad por medio de análisis de sangre
en la que se comprueba las alteraciones provocadas por la enfermedad
o también ( aunque mas difícilmente), viendo los tripanosomas.La
mayor parte de las personas permanece en este periodo todo el resto
de sus vidas, y aun hay quienes han curado espontáneamente.
Periodo Crónico
Por lo general es una manifestación tardía de la infección.
Se la encuentra en casi un 15% de quienes han padecido el contagio
y sus manifestaciones mas evidentes están en la relación
directa con las alteraciones del corazón. Sus síntomas
mas comunes son: palpitaciones, disnea, dolores referidos al área
cardiaca, dolor en la zona hepática y sobre todo, manifestaciones
típicas que se observan en el electrocardiograma, aunque
no haya síntomas clínicos.
La mayor parte de los síntomas son indicación de
daño cardiaco, que cuando es importante lleva a grados variables
de insuficiencia cardiaca. La gravedad del proceso es variable,
pero lo que le da la característica alarmante es la frecuencia
con que el daño cardiaco se produce. Si tenemos en cuenta
que hay regiones del país de las cuales la mayor parte de
la población esta infectada con Trypanosoma Cruzi, el porcentaje
que resulta con lesión cardiaca da una cifra que justifica
todo esfuerzo para combatir el mal de Chagas.
Otro dato a tener en cuenta es que la cardiopatía chagásica
se produce en personas jóvenes; es decir que, teniendo un
organismo relativamente sano, presenta invalidez para la vida normal
debido a la lesión del corazón. El Trypanosoma Cruzi
afecta también al sistema nervioso, al aparato digestivo,
al sistema muscular, etc
Tratamiento
Los dos medicamentos que actualmente existen en el mercado son el
Nifurtimox y el Benznidazol.
Existe unanimidad de criterios en cuanto a la aplicación
inmediata de estos medicamentos en la fase aguda de la enfermedad.
Ello no ocurre en lo que refiere a la fase crónica de la
enfermedad, donde algunos autores tienen sus dudas en cuanto a la
eficacia de su administración, sobre todo teniendo en cuenta
la posibilidad, nada despreciable, de que aparezcan efectos secundarios
de cierta importancia.
Profilaxis de la enfermedad de Chagas
Con relación a las medidas mas plausibles para la prevención
de la Trypanosoma Cruzi humana siguen en pie las proposiciones formuladas
en 1938 por Salvador Mazza en el VI Congreso Nacional de Medicina
( Córdoba), ampliadas por Mazza y Jorg en 1940 y reiteradas
por Jorg en 1959 en el 6to Congreso Médico Social de la Confederación
Medica Panamericana, que pueden enunciarse en los siguientes principios
generales con proyección sanitaria:
Ha de procederse a un estudio y a medidas de acción general
para lograr la modificación fundamental de la vivienda rural
y ciudadana infectada por vinchucas o susceptible de serlo. Comprende
la erradicación del rancho con todas sus implicancias de
deformación social y familiar y la creación de modelos
de habitaciones higiénicas adaptadas tanto a las posibilidades
materiales y económicas, como al uso, clima y particularidad
de cada región y cada comunidad.
Ha de ponerse en marcha un programa y una acción de Educación
Sanitaria, en todos los niveles y por todos los medios, inicial
y fundamentalmente por el escolar y el trabajo social-sanitario
directo, hasta llevar el conocimiento de la enfermedad, sus riesgos
y su profilaxis, a la mayor masa de población posible.
Tratar de cortar la cadena morbígena, actuando sobre el
punto mas accesible: impedir el desarrollo domiciliario y destruir
la vinchuca en todos sus periodos de desarrollo en la habitación
humana y su entorno, con un insecticida lo mas especifico posible,
de acción prolongada, residual, de costo accesible y de mínimo
riesgo de toxicidad para el hombre y los animales domésticos.
Modificación del biotipo peridomiciliario para alejar los
hospedadores y transmisores silvestres de la vivienda humana; ademas
para evitar durante los rociados insecticidas de las casas, las
vinchucas encuentren refugio en el entorno y, en suma, para crear,
en todo alcance, condiciones ecológicas generales adversas
para la perpetuación de la cadena morbígena de la
Trypanosoma Cruzi.
A continuación editaremos el Trabajo del Dr.Sergio Sosa Estani
Desde la década de 1930 fue investigado el tratamiento
específico de la enfermedad de Chagas. Las metas del tratamiento
específico contra la infección por Trypanosoma Cruzi,
son a nivel individual, eliminar el parásito y disminuir
la probabilidad de desarrollar la enfermedad. A fines de los años
?60 y principios de los ?70, dos compuestos químicos fueron
evaluados por ensayos clínicos en Argentina: Nifurtimox y
Benznidazol. Después de la aprobación de su uso por
la Autoridad de Regulación del Ministerio de salud, en 1983
fue escrita y aprobada la primera Norma para el tratamiento de la
infección por T. Cruzi. Esta Norma recomendó procedimientos
para tratar los casos en Fase Aguda de enfermedad de Chagas. Debido
a la publicación de nueva información que soporta
la utilización de estas drogas para el tratamiento de casos
en fase indeterminada de la enfermedad de Chagas, en 1997 la Norma
original fue revisada y fue aprobado un nuevo procedimiento (Resolución
Secretaría de programas de Salud/Ministerio de Salud y Acción
Social de la Nación N° 28/99). Actualmente el tratamiento
es recomendado en: 1) Todo paciente en Fase Aguda de la enfermedad
de Chagas, 2) Niños y adolescentes en fase Indeterminada
de la enfermedad de Chagas. 3) Pacientes adultos en fase Indeterminada
o con una forma cardiaca incipiente sintomática de la enfermedad
de Chagas. 4) Accidentes con material contaminado en laboratorio
o durante cirugías. 5) Donante o receptor en transplantes
de órganos. Es necesario realizar el acompañamiento
médico y laboratorio clínico general durante el tratamiento
para monitorear al paciente. La titulación de anticuerpos
específicos con antígenos monoespecíficos mostró
ser un marcador apropiado para la eficacia terapéutica.
En la infección por Trypanosoma Cruzi (T. Cruzi) que causa
la enfermedad de Chagas se distinguen 3 fases de evolución
clínica. En cada una de ellas la presentación clínica,
los criterios diagnósticos y terapéuticos son diferentes1.
La fase aguda se inicia al momento de adquirir la infección
y se desarrolla durante 2 a 4 meses. Se caracteriza porque el paciente
presenta apreciable parasitemia detectada en forma directa, un perfil
clínico presente en todos los casos, con características
ines-pecíficas y específicas (5% de los casos)2. La
fase indeterminada o Latente corresponde a la etapa que sigue a
la fase aguda. Se caracteriza porque el paciente no presenta síntomas
ni signos viscerales, presenta estudios serológicos reactivos
y raramente estudios parasitológicos- directos positivos.
El paciente permanece toda la vida en esa etapa, o deriva a la Fase
Crónica con alguna manifestación orgánica al
cabo de aproximadamente 10 a 30 años. En este caso el paciente
se halla en la fase crónica, los síntomas y/o signos
son de expresión variada, siendo la forma cardiaca la más
frecuente. Este paciente se denomina enfermo chagásico. El
paciente en la fase indeterminada se denomina infectado chagásico.
El tratamiento específico contra el Trypanosoma Cruzi tiene
como objetivo dirigido al individuo, curar la infección y
disminuir la probabilidad de desarrollar la enfermedad de Chagas1,
3.
Desde la década de los años 1930 se realizaron intentos
para obtener una droga apropiada para el tratamiento de la infección
por Trypanosoma Cruzi. En forma experimental se han utilizado cerca
de un centenar de compuestos, de los cuales solamente algunos superaron
la etapa preclínica4. Son de destacar, la bisquinaldina,
utilizada por Mazza en 1937, el Cruzón, los derivados de
la 8-Aminoquinolina sintetizados en 1949 (Primaquina, Moxipraquina),
5-Nitrofuranos sintetizados en 1952 (Nitrofurazona, Nifurtimox),
derivados de 5-Nitroimi-dazoles sintetizados en 1961 (Metronidazol),
5-Nitro-tiazoles sintetizados en 1966 (Niridazol), los 2-Nitroi-midazoles
sintetizados en 1968 (Benznidazol), y el Allopurinol, droga propuesta
en los últimos años para el tratamiento en la fase
indeterminada. De las sustancias mencionadas anteriormente, completaron
la investigación clínica el Nifurtimox (1972) y el
Benznidazol (1974) que fueron aprobadas por el Ministerio de Salud
y Acción Social de la Nación como drogas anti-T. cruzi.
Ambas drogas se probaron para la fase aguda de la infección,
en la indeterminada y posteriormente en la fase crónica.
A fines de los años 60 y principios de los 70, dos compuestos
químicos fueron evaluados por ensayos clínicos en
Argentina: Nifurtimox y Benznidazol. Después de la aprobación
de su uso por la Autoridad de Regulación del Ministerio de
Salud, en 1983 fue escrita y aprobada la primera Norma5 para el
tratamiento de la infección por T. Cruzi. Esta Norma recomendó
procedimientos para tratar los casos en fase aguda de enfermedad
de Chagas. Debido a la publicación de nueva información
que soporta la utilización del Benznidazol para el tratamiento
de casos en fase indeterminada de la enfermedad de Chagas, en 1997
la Norma original fue revisada y fue aprobado un nuevo procedimiento
(Resolución Secretaría de programas de Salud/Ministerio
de Salud y Acción Social de la Nación N° 28/99).
Las experiencias
En la experiencia con pacientes cursando la fase aguda, el tratamiento
con Nifurtimox, utilizando los esquemas protocolizados, se observaron
la negativización parásito-lógica directa y
el xenodiagnóstico, así como la serología a
los 4 meses y 12 meses posteriores al tratamiento6, 7. Sin embargo
con el esquema aprobado en las Normas de 1983, se observaron negativización
del xenodiagnós-tico entre el 88 y 100% de los casos evaluados
entre 8 y 123 meses de seguimiento y a diferencia del tratamiento
de la fase crónica en que solamente entre los pacientes de
6-10 años de edad, se observó negativización
serológica8. En algunos de los pacientes se encontró
negativización serológica variable entre el 28 y 38%
de los casos6, 8, 9, 10. Estos resultados y la hipótesis
de la autoinmunidad como único mecanismo lesionante en la
enfermedad de Chagas crónica, provocaron que en 1983 se recomendó
tratar exclusivamente los pacientes con enfermedad de Chagas en
fase aguda, tanto en Brasil como en Argentina. Con esta recomendación
se interrumpieron las investigaciones, a pesar que diferentes autores8,
10, 11, 12, 13, 14, 15, concluyeron que estas drogas eran efectivas
también en la fase indeterminada. En la mayoría de
las series de tratamiento la serología persistió reactiva
en los pacientes11, 13, 14. Algunos autores indicaron disminución
de títulos serológicos en los pacientes tratados3,
12, 16, 17, 18. Algunos autores explicaron la persistencia serológica
por la posibilidad que no haya un «clearance» total
de parásitos en el organismo14, 16. También se ha
interpretado la persistencia serológica, debido a la existencia
de familias de anticuerpos que por una parte se detectan por serología
y otros que aparecerían solamente en presencia de la infección,
como manifestación de la resistencia del huésped y
que desaparecerían después de la aplicación
del tratamiento específico al paciente19, 20.
En 1994 Viotti et al.17 describieron en 131 pacientes adultos jóvenes
tratados con Benznidazol y 70 pacientes no tratados (controles)
con edades entre 9 y 73 años y un seguimiento en media de
8 años, la evolución serológica, electrocardiográfica
y clínica. En este trabajo se describió que el 30%
de los controles tuvo cambios electrocardiográficos desfavorables,
mientras que esas alteraciones se comprobaron en 4.2% de los pacientes
tratados (p < 0.05). La negativización serológica
expresada a través de 3 técnicas no reactivas, se
observó en 19.1% de los pacientes tratados y en 6% de los
controles. La evolución clínica desfavorable según
la clasificación de Kuschnir ocurrió en 17 y 2.1%
de pacientes controles y tratados respectivamente (p < 0.05).
En aquellos pacientes que negativizaron la serología, independientemente
del tratamiento, no se observaron alteraciones electrocardiográficas.
En cambio, entre los que mantuvieron la serología reactiva
se observaron alteraciones del ECG en el 29% de los pacientes controles
y 2% de los tratados con Benznidazol. Los autores concluyen que
el tratamiento ejerce un efecto protector en la etapa crónica
de la infección.
Entre 1991 y 1995 se llevó a cabo un ensayo clínico
controlado para evaluar la eficacia del tratamiento con Benznidazol
en niños con fase indeterminada de la infección3.
En este estudio que incluyó 55 niños tratados con
Benznidazol y 51 niños con placebo se evaluó a través
de serología, parasitología, electrocardiografía
y clínica en un seguimiento de cuatro años. Este estudio
demostró en cuatro años de seguimiento una disminución
significativa de los títulos de Ac en los pacientes que recibieron
Benznidazol, a través de las técnicas de hemoaglutinación
indirecta (HAI), inmunofluorescencia indirecta (IFI) y ELISA utilizando
antígeno total, mientras que no se observaron cambios en
los que recibieron placebo. Entre los pacientes que mostraron reactividad
de Anticuerpos (Ac) contra el Antígeno (Ag) recombinante
F2921 se demostró un porcentaje de negativización
de 62.1% al final del seguimiento entre los niños tratados
con Benznidazol y ninguna disminución entre los que recibieron
placebo3. Otros autores en Brasil encontraron resultados similares
usando Ag no usados en serología convencional18, 22, 23,
24. El xenodiagnóstico al final del seguimiento fue de 4.7%
entre los tratados con Benznidazol y 51.2% entre los controles (p
< 0.05). Este trabajo concluyó que la eficacia superó
el 60% y que fue posible el tratamiento de forma ambulatoria en
niños residentes en áreas rurales. Se cuantificó
la concentración plasmática de p-Selectina (Molécula
de Adhesión), que se observa significativa-mente aumentada
en pacientes con infección por T. Cruzi.25. La cuantificación
de p-Selectina por inmuno ensayo enzimático, al finalizar
el tratamiento en los pacientes de este ensayo clínico resultó
ser significativamente menor en los pacientes tratados con Benzidazol
comparados con los controles26.
En Brasil otro ensayo controlado en niños en edad escolar18
tratados con Benznidazol o placebo mostró resultados coincidentes
a los observados en Argentina. La evolución serológica
evaluada a través de una ELISA por quimioluminiscencia utilizando
Ag de trypomastigote27 demostró una negativización
en 63.8% y 5.5% de los pacientes tratados con Benznidazol y placebo
respectivamente, luego de 36 meses de seguimiento.
En los últimos años, aunque sin diseño controlado,
se documentaron observaciones que demostraron reproducir los resultados
mencionados anteriormente. En 1993 se describió en la provincia
de Santa Fe, la evaluación parasitológica con xenodiagnóstico
y evolución serológica a través de HAI, IFI
y Aglutinación Directa, en niños tratados durante
la fase indeterminada de la infección28. En 29 niños
la posibilidad de los xenodiagnósticos pretratamiento y post-tratamiento
fue de 79.3 y 0% respectivamente con una media de 3 xenodiagnósticos
por niño. El seguimiento con una mediana de 9 años
en 35 niños permitió observar negativización
serológica en 63% de los casos. Este mismo grupo29 describió
la evolución de 74 pacientes infectados por T. Cruzi, jóvenes
con edad entre 21 y 30 años con un seguimiento mayor a 15
años. La evolución serológica por IFI mostró
en 37 pacientes tratados y 37 no tratados (controles) que en el
94% de los pacientes tratados los títulos fueron £
1/64, mientras que en el 67% de los controles fue ³ 1/128,
con valores de la media geométrica de los títulos
significativamente menores en los pacientes tratados comparado con
los controles. Dos pacientes tratados mostraron negativiza-ción
serológica en las 3 reacciones. En el oeste de Santiago del
Estero se describió30 la evolución serológica
con HAI y ELISA convencional en 147 niños entre 1 y 14 años
seguidos durante 20 meses. Los resultados obtenidos mostraron una
negativización serológica de 49.3% entre 75 niños,
32.7% ente 61 niños y 0% entre 11 niños de 0-4; 5-9
y 10-14 años de edad, respectivamente.
Estos últimos estudios descriptos, aunque sin diseño
controlado pero realizado por grupos independientes, muestran resultados
similares a los observados por los estudios basados en diseños
controlados.
Efectos adversos
Diferentes autores refieren que los efectos adversos aparecen entre
el 4 y 30% de los casos2, 3, 30, 31, 32, agrupados en manifestaciones
dérmicas (exantema morbiliforme), gastrointestinales (epigastrálgias,
cólicos, náuseas, vómitos), neurotoxicidad
central (irritabilidad nerviosa, insomnio, cefaleas, anorexia),
y periférica (parestesia, hiperestesia), mioartralgias. Controles
de laboratorio mostraron valores de bilirrubina normales, pudiéndose
observar elevaciones de transaminasas3, 7, 32. Excepcionalmente
se pueden observar alteraciones hematológicas con leucopenia
o plaquetopenias33. Los efectos adversos están directamente
relacionados con la dosis y la edad del paciente, siendo más
tolerada en niños y lactantes que por adolescentes y adultos9,
14, 34. En nuestra experiencia en todos los casos los efectos adversos
desaparecen al disminuir la dosis o suspender el tratamiento. De
cualquier manera el tratamiento exi-ge una supervisión médica
directa durante su realización35.
Evaluación del tratamiento
Para evaluar la respuesta a la quimioterapia específica,
es recomendable utilizar la combinación diagnóstica,
clínica, inmunoserológica y parasitológica.
En los últimos años se ha demostrado en Argentina3,
21, 36 y otros países como Brasil18, 22, 23, 24, 27, la utilización
de nuevas herramientas para la evaluación de la eficacia
del tratamiento, que se complementan a las ya existentes como son
la utilización de Ag recombinantes o Ag de tripomastigote,
como también la reacción en cadena de la polimerasa
(PCR)37, 38. Asimismo, a la luz de los conocimientos actuales, es
necesario considerar en la eficacia antiparasitaria del tratamiento,
la ausencia del parásito y la disminución significativa
de la concentración de Ac o hasta la negativización
de la serología. Se debe tener en cuenta la limitación
de los estudios parasi-tológicos como los métodos
de Strout y el xenodiagnóstico en la evaluación del
tratamiento en las fases indeterminada y crónica debido a
la baja sensibilidad en ambos métodos en esta fase y la complejidad
del xenodiagnóstico para su realización.
Situación actual
El Programa de Chagas en Argentina, desde 1994 ha incorporado el
Subprograma «Detección y tratamiento en niños
de 0 a 14 años de edad infectados por Trypanosoma Cruzi.»,
que consiste en la detección de niños infectados por
T. Cruzi, entre los residentes en las viviendas que están
bajo la vigilancia entomológica, condición necesaria
para la indicación del tratamiento39.
En 1997 fueron revisadas las normas de atención del infectado
chagásico en Argentina y los presentes criterios han sido
elaboradas teniendo en cuenta resultados comprobados mediante investigaciones
científicas sobre atención médica, apoyo asistencial
y tratamiento del paciente chagásico, basadas fundamentalmente
en la experiencia obtenida por el uso del Benznidazol. Actualmente
en las «Normas de Atención del Infectado Chagásico
(N° resolución 28/99 de la Secretaría de Programas
de Salud/Ministerio de Salud y Acción Social de la Nación)
el tratamiento se recomienda en: a) Todo paciente en fase aguda
de la enfermedad de Chagas, b) Niños y adolescentes en fase
indeterminada, c) Pacientes adultos en fase indeterminada o con
una forma cardiaca incipiente sintomática de la enfermedad
de Chagas, d) Accidentes con material contaminado en laboratorio
o durante cirugías y e) donante o receptor en trasplantes
de órganos. Es necesario realizar el acompañamiento
médico y laboratorio clínico general durante el tratamiento
para monitorear al paciente.
El actual criterio de atención del infectado chagásico
aplicado en el marco de las acciones del Programa Nacional de Control
de Chagas, contempla detectar precozmente a la población
infantil infectada por T. Cruzi. El diagnóstico precoz y
el tratamiento oportuno en las primeras décadas de la vida
permiten curar y prevenir la ocurrencia de la enfermedad mejorando
el pronóstico y la calidad de vida
Por: Dr.
Luis A. Seambelar

